摘要:量热仪的操作步骤包括准备阶段、操作阶段和结束阶段。需准备量热仪、样品、燃烧杯等,并检查仪器状态。按照开机、输入样品信息、放置样品、点燃、记录数据和关机等步骤操作仪器。清理仪器和实验环境。整个操作过程需严格遵守安全规范,确保实验的准确性和可靠性。
本文目录导读:
实验目的
掌握燃烧量热仪测定物质燃烧热的基本原理和操作方法,了解物质燃烧反应热效应的影响因素,通过本实验进一步加深对燃烧焓概念的理解,学习绘制燃烧反应热量与时间的曲线图。
实验原理
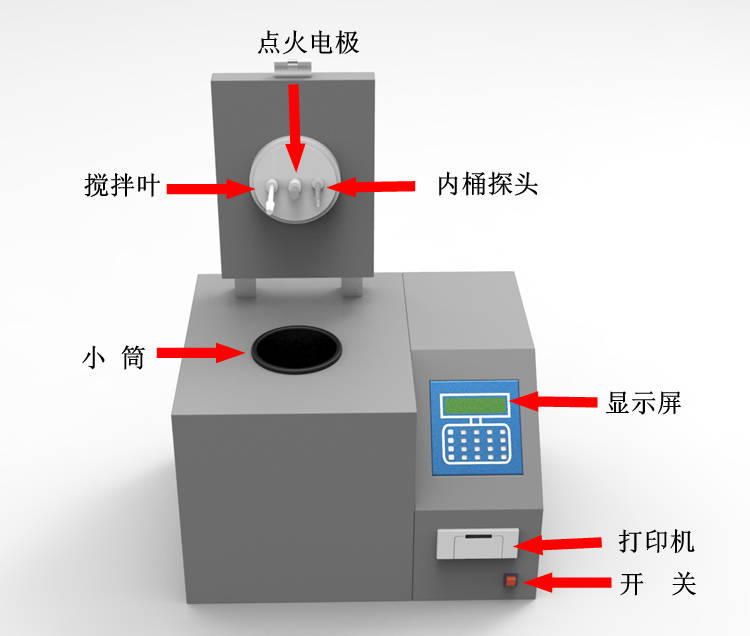
燃烧量热仪是用来测定物质燃烧热的仪器装置,在一定的压力条件下,通过精确测量一定量燃烧剂完全燃烧时释放出的热量来确定物质的燃烧热,本实验采用氧弹量热法,将装有样品和过量氧气的氧弹插入已知质量的量热计中,在恒温条件下,测定燃烧过程中释放的热量,通过测定水在燃烧过程中升高的温度来计算样品的燃烧热,本实验装置主要由氧弹、燃烧室、搅拌器、测温装置及水浴恒温装置等组成,氧弹由铜质材料制成,其外壳为耐压钢筒,内部装有一定量的水作为传热介质,样品在氧弹内燃烧时产生的热量被水吸收,水的温度升高,通过测量水温升高的数值来计算样品的燃烧热,本实验采用积分法测量热量,即测量一定时间内水温的变化值ΔT,通过计算ΔT对应的热量值来计算样品的燃烧热,实验中还可以绘制热量与时间的曲线图来分析实验数据。
仪器装置和材料
燃烧量热仪、氧弹、搅拌器、温度计、恒温水浴装置、电子天平(精度为0.0001g)、样品(如苯甲酸)、氧气瓶等。
操作步骤
实验前准备:检查仪器装置是否完好,确保各部件安装正确无误,打开恒温水浴装置,设定温度为实验所需温度(如25℃),用电子天平称量样品质量(精确到小数点后四位),记录样品质量数据,准备足够的氧气瓶,确保氧气供应充足,将温度计插入量热计中,确保测温装置正常工作,将搅拌器放入量热计中,确保搅拌器能够正常工作并搅拌均匀水介质,将氧弹插入量热计中,确保密封良好且无漏气现象,开始实验:打开氧气瓶阀门,向氧弹内注入适量氧气(注意氧气压力不要过高),将量热计置于恒温水浴中,确保水温恒定并记录初始水温T1,启动搅拌器,使水介质充分搅拌以保证热量均匀传递,点燃氧弹内的样品,观察并记录燃烧过程,当燃烧结束后,记录最终水温T2和燃烧时间t(从点燃样品开始至火焰熄灭的时间),计算ΔT = T2 - T1,根据公式Q = mcΔT计算样品的燃烧热(其中m为水的质量,c为水的比热容),绘制热量与时间的曲线图:以时间为横坐标,热量为纵坐标,绘制出样品燃烧过程中热量与时间的关系曲线图,分析实验结果:根据实验数据和曲线图分析样品的燃烧特性及影响因素,整理实验数据并撰写实验报告,实验结束后:关闭氧气瓶阀门和恒温水浴装置,清理仪器装置和实验室环境,确保安全,将使用过的器材归位并整理好实验室。
注意事项
1、实验过程中要注意安全,避免氧气泄漏和高温烫伤等危险情况发生。
2、氧弹内的氧气压力不要过高,以免发生爆炸危险。
3、恒温水浴的温度要控制好,确保水温恒定并符合实验要求。
4、点燃样品时要迅速点燃并确保火焰稳定燃烧,避免样品飞溅或不完全燃烧等情况发生。
5、实验过程中要记录准确的数据和观察现象,以便后续分析和计算。
6、实验结束后要及时清理仪器装置和实验室环境,确保安全和整洁。
实验结果与数据分析
根据实验数据和曲线图分析样品的燃烧特性及影响因素,可以分析不同样品在相同条件下的燃烧热差异以及不同条件下同一样品的燃烧热变化等,通过对比实验数据和理论值可以评估实验的准确性和可靠性,并进一步探讨误差来源及影响因素,通过对实验结果的分析可以深入了解物质的燃烧反应热效应及其影响因素,加深对燃烧焓概念的理解,同时还可以通过绘制热量与时间的曲线图直观地展示实验结果和分析过程,最后整理实验数据并撰写实验报告以便后续查阅和交流讨论,通过本实验操作过程的实践可以提高学生的实验操作能力和科学素养培养严谨的科学态度和方法论意识为后续学习和工作打下坚实的基础,同时也有助于培养学生独立思考和解决问题的能力提高综合素质和实践能力为未来的科学研究和社会服务做出贡献,总之掌握量热仪的操作步骤对于学习化学和物理学科的学生来说是非常重要的一个实验技能通过实验操作和数据分析可以加深对相关理论知识的理解和掌握提高实验操作能力和科学素养为未来的学习和工作打下坚实的基础。



 京公网安备11000000000001号
京公网安备11000000000001号 京ICP备11000001号
京ICP备11000001号
还没有评论,来说两句吧...